Die Änderung folgt der Auswertung von Berichten durch die FDA, in denen "seltene, aber schwerwiegende" Vorfälle beschrieben wurden, die auftraten, als Benutzer dieser Medikamente ein komplexes Schlafverhalten erlebten: Schlafwandeln, Schlaftreiben "und andere Aktivitäten ausführen, während sie nicht vollständig wach waren", schrieben Vertreter der FDA gestern (30. April) ) in einer Ankündigung zur Arzneimittelsicherheit.
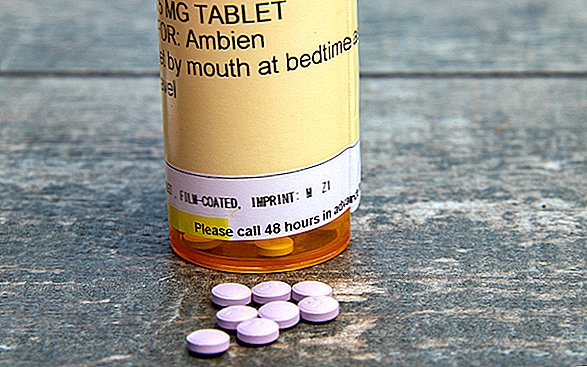
Laut Ankündigung wird jetzt in den Leitfäden für Patientenmedikamente und in den Verschreibungsinformationen für Schlaflosigkeitsmedikamente wie Ambien (Gattungsname Zolpidem), Sonata (Gattungsname Zaleplon), Lunesta (Gattungsname Eszopiclon) und andere eine markante Warnung angezeigt.
Eine weitere der strengsten Warnungen der FDA - eine Kontraindikation, die die Vermeidung eines Arzneimittels unter bestimmten Bedingungen empfiehlt - wird ebenfalls enthalten sein und Personen, die bereits ein komplexes Schlafverhalten bei der Verwendung dieser Arzneimittel erfahren haben, auffordern, den Gebrauch abzubrechen.
Die FDA untersuchte Daten aus 26 Jahren und fand 66 Beispiele für komplexes Schlafverhalten im Zusammenhang mit diesen Medikamenten. Die Patienten führten Maßnahmen durch, die nach extremer Kälte zu Unterkühlung oder Gliedmaßenverlust führten. Es gab Fälle von Kohlenmonoxidvergiftung, Ertrinken, offensichtlichen Selbstmordversuchen, selbst zugefügten Schusswunden und Autounfällen - mit dem Patienten am Steuer.
In den meisten Fällen erinnerten sich die Patienten laut FDA nicht einmal an die Vorfälle, die zu ihren Verletzungen führten.
Da diese Ergebnisse nur auf Fallberichten in der medizinischen Literatur und Berichten beruhten, die direkt an die FDA gesendet wurden, ist es möglich, dass es noch mehr Beispiele für Verletzungen durch komplexes Schlafverhalten gibt, die nicht dokumentiert wurden, sagten FDA-Beamte.
Millionen Amerikaner leiden an Schlaflosigkeit und sind auf Medikamente angewiesen, um besser schlafen zu können. "Es ist jedoch wichtig, dass Patienten und Angehörige der Gesundheitsberufe sich des Risikos bewusst sind", sagte der amtierende Kommissar der FDA, Dr. Ned Sharpless, in einer Erklärung.
"Diese Vorfälle können nach der ersten Dosis dieser Schlafmittel oder nach einer längeren Behandlungsdauer auftreten und können bei Patienten ohne Vorgeschichte dieser Verhaltensweisen und sogar bei den niedrigsten empfohlenen Dosen auftreten", sagte Sharpless.
Es ist nicht gut verstanden, wie diese Medikamente komplexe Schlafverhalten auslösen, die zu Verletzungen führen können, sagten FDA-Beamte. Die Agentur wird weiterhin Medikamente gegen Schlaflosigkeit überwachen und die damit verbundenen Risiken bewerten, um festzustellen, ob weitere Maßnahmen erforderlich sind, sagte Dr. Janet Woodcock, Direktorin des FDA-Zentrums für Arzneimittelbewertung und -forschung, in der Erklärung.












